Содержание:
Коррозия металлов
При металлизации на поверхность направляется ионизированный дуговой поток мелкодисперсного напыляемого металла, а легирование реализуется в процессе выплавки металла, как следствие протекания металлургических реакций между основным металлом и вводимыми легирующими добавками.
В некоторых случаях существенного снижения коррозии удаётся добиться изменением состава атмосферы, в которой работает защищаемая металлоконструкция.
Это может быть вакуумирование для сравнительно небольших объектов , или работа в среде инертных газов аргон, неон, ксенон. Данный метод весьма эффективен, однако требует дополнительного оборудования — защитных камер, костюмов для обслуживающего персонала и т. Используется он главным образом, в научно-исследовательских лабораториях и опытных производствах, где специально поддерживается необходимый микроклимат.
Новое на сайте
В завершение укажем и на довольно необычный способ коррозионной защиты: с помощью самих окислов железа, точнее, одного из них — закиси-окиси Fe3O4. Данное вещество образуется при температурах …С и по своим механическим свойствам представляет собой высоковязкую технологическую смазку.
Это явление используется при скоростной высадке труднодеформируемых металлов и сплавов. Эффективность данного способа обусловлена тем, что при каждом технологическом цикле контактные поверхности обновляются, а потому стабильность процесса регулируется автоматически. Что такое коррозия и её разновидности Основной причиной интенсивного окисления поверхности металлов что и является основной причиной коррозии являются: Повышенная влажность окружающей среды.
Химическая коррозия
Наличие блуждающих токов. Неблагоприятный состав атмосферы. Схема работы Оставляете заявку на сайте или по телефону. Оцениваем запрос и тех.
Коррозия неметаллических материалов
По мере ужесточения условий эксплуатации (повышение температуры, механических напряжений, агрессивности среды и др.) и неметаллические материалы подвержены действию среды. В связи с чем термин «коррозия» стал применяться и по отношению к этим материалам, например «коррозия бетонов и железобетонов», «коррозия пластмасс и резин». При этом имеется в виду их разрушение и потеря эксплуатационных свойств в результате химического или физико-химического взаимодействия с окружающей средой. Но следует учитывать, что механизмы и кинетика процессов для неметаллов и металлов будут разными.
Протекторная защита от электрохимической коррозии
Как упоминалось выше, чем больше потенциал металла, тем быстрее происходит электрохимическая коррозия. Значит, снижая электрический потенциал, можно добиться наступления момента, когда процесс окисления станет невозможным. На этом принципе основана протекторная или, другими словами, электрохимическая защита металлических конструкций, газопроводов, корпусов морских судов. Берется такой металл, который ведет себя активнее, нежели основной защищаемый, и соединяется с последним токопроводящим проводником. Получается, что уже этот анод вступает в реакцию с коррозионной средой, а основной металл остается невредимым.
Основные случаи, когда применение протекторной защиты будет оправдано:
- Недостаточно средств на проведение более дорогостоящих защитных мероприятий.
- Если защитой нужно обеспечить конструкции из металла небольших габаритов.
- Когда трубопроводы имеют дополнительную поверхностную изоляцию.
Такую защиту от электрохимической коррозии, как протекторная, применяют, в основном, к разным маркам стали. Здесь уместным будет использование протекторов на основе кадмия, алюминия, магния, хрома, цинка, но используется не чистый элемент, а сплавы.
Цинковые протекторы
Цинковые протекторы, кроме основы из цинка, содержат:
- до 0.15% кадмия при минимально возможном процентном соотношении в 0.025%;
- до 0.5% алюминия;
- примеси железа, свинца и меди, общей суммой не превышающие 0.005%.
Наиболее эффективное применение цинка выявлено в морской воде, где с помощью таких протекторов успешно работает защита, например, газовых или нефтяных магистралей. Плюс цинка еще в том, что он допустим к использованию со взрывоопасными веществами. Когда происходит растворение анода, не наблюдается выделения загрязняющих веществ, которые могут навредить экологии.
Применение цинковых протекторов в водоемах, где вода имеет пресный состав либо в грунте под землей сопровождается быстрым образованием на поверхности протектора таких соединений, как оксиды и гидроксиды, которые приводят к торможению электрохимического процесса окисления анода, и фактически прекращается защита основного металла от электрохимической коррозии.
Установка цинкового протектора на днище корабля:

Магниевые протекторы
В чистом виде магниевые протекторы нецелесообразно применять, что объясняется быстрым ржавлением этого металла. Поэтому коррозионные защитники на базе магния, кроме него, имеют:
- максимум 5%, минимум 2% цинка;
- максимум 7%, минимум 5% алюминия;
- небольшое содержание меди, никеля и свинца, не более десятых долей процента.
Протекторы из магния хороши, когда среда, в которой они применяются, имеет pH не выше 10.5, что соответствует грунтам обычного характера, водным объектам со слабосоленой акваторией либо попросту пресной воде. Для защиты подходят любые трубопроводы и металлоконструкции, находящиеся в описанных выше условиях. Применение магния в агрессивных соленых растворах сопровождается быстрым образованием плохо растворимой пленки на его поверхности.
Алюминиевые протекторы
Целевое назначение протекторов из алюминия – работать в качестве защиты от электрохимической коррозии в средах с водой проточной с соленым составом, например, в прибрежных морских водах. В составе сплава протектора из алюминия имеются:
- примеси индия, кадмия, кремния не более 0.02%;
- цинка – до 8%;
- магния – до 5%.
Благодаря этим дополнительным металлам нет возможности появления на протекторе жесткой, задерживающей растворение пленки. Допустимо применять алюминиевый протектор и в средах, подходящих для магниевого протектора.
Защита
При постоянном взаимодействии с химическими элементами окружающей среды металл со временем истончается, становится хрупким, шершавым. Такой металл нельзя использовать в производстве. Поэтому были разработаны способы защиты металла от коррозии.
Сохранить металлические свойства и продлить срок службы металлическим изделиям можно с помощью:
- металлического покрытия – нанесения тонким слоем других металлов;
- неметаллического покрытия – изоляции металла от окружающей среды органическими или неорганическими веществами – лаками, эмалью, пластмассой, резиной, красками;
- электрохимической защиты – наложения постоянного электрического поля;
- ингибиторной защитой – нанесения ингибиторов для защиты металла в кислой среде.
Металлическое покрытие бывает двух видов:
- катодное – покрытие пассивными металлами (Ni, Sn, Ag, Au);
- анодное – покрытие активными металлами (Zn, Cr).

Рис. 3. Оцинкованное железо.
Морские суда защищают пластинами, сделанными из более активных металлов (алюминия, магния, цинка), чем корпус корабля.
Металл также защищают «изнутри», добавляя в состав коррозиестойкие химические элементы. Например, нержавеющая сталь содержит хром, углерод, кремний, серу, фосфор, марганец.
Что мы узнали?
Из урока химии 9 класса узнали о коррозии, её видах и способах защиты. Коррозия – саморазрушение металла под воздействием факторов окружающей среды, к которым относится воздействие кислорода, водорода, кислот, щелочей. Под действием внешних элементов поверхность металла окисляется, становится тонкой и хрупкой. Тема коррозии важна для производства сплавов и металлических изделий. Чтобы продлить срок службы, в металл добавляют устойчивые к коррозии элементы или покрывают поверхность другими металлами, органическими или неорганическими веществами, ингибиторами.
-
Вопрос 1 из 10
Начать тест(новая вкладка)
Ржавеют… все!
Выше в статье упоминался такой известный центр борьбы с коррозией, как Шведский институт коррозии (ШИК) — одна из наиболее авторитетных организаций в данной области.
Раз в несколько лет ученые института проводят интересное исследование: берут кузова хорошо потрудившихся автомобилей, вырезают из них наиболее подверженные коррозии «фрагменты» (участки порогов, колесных арок, кромок дверей и т.д.) и оценивают степень их коррозионного поражения.
Важно отметить, что среди исследуемых кузовов есть как защищенные (оцинковкой и/или антикором), так и кузова без какой либо дополнительной антикоррозионной защиты (просто окрашенные детали). Так вот, ШИК утверждает, что наилучшей защитой автомобильного кузова является лишь сочетание «цинк плюс антикор»
А вот все остальные варианты, включая «просто оцинковку» или «просто антикор», по словам ученых — плохи
Так вот, ШИК утверждает, что наилучшей защитой автомобильного кузова является лишь сочетание «цинк плюс антикор». А вот все остальные варианты, включая «просто оцинковку» или «просто антикор», по словам ученых — плохи.
Виды
Коррозия может происходить в присутствии электролитов и неэлектролитов. Поэтому основными видами коррозии металлов по механизму возникновения являются:
- химическая – возникает в отсутствии электролита в сухой или влажной среде;
- электрохимическая – происходит в присутствии электролита.
Химическая коррозия связана с неэлектролитами – веществами, не проводящими электрический ток в растворах или расплавах. К неэлетролитам относятся многие простые неорганические (кислород, водород) и органические (эфир, бензол) вещества.
Химическая коррозия может происходить в присутствии газов (водорода, кислорода, хлора), органических кислот и солей. Молекулы металла соединяются с химическими элементами, и на металлической поверхности возникают плёнки – оксиды, сульфиды, гидриды. Внешне это заметно по изменению цвета. Железо, соединяясь с кислородом, образует Fe2O3 – оксид железа (III) – рыжую ржавчину.
Рис. 2. Оксид железа.
Если в расплаве или в растворе присутствуют вещества, проводящие электрический ток (электролиты), то появляется электрохимическая коррозия. Она возникает в присутствии солей, кислот, щелочей или при соприкосновении поверхностей двух металлов, между которыми находится влажная среда. Из-за разности окислительно-восстановительных потенциалов возникает гальванический элемент – источник электрического тока. Металл выступает в роли анода (восстановителя), электролит – катода (окислителя). Анод, отдавая электроны, окисляется или коррозирует.
Рис. 3. Схема электрохимической коррозии.
Классификация коррозии может проводиться по другим признакам. По очагу поражения коррозия бывает:
- местной;
- сплошной;
- точечной.
Коррозия может происходить в разных средах:
- газовой (безводной);
- атмосферной (влажной);
- жидкостной;
- грунтовой;
- радиационной.
Соль ускоряет процесс ржавления, поэтому корабли быстрее ржавеют в морской, чем в пресной воде.
Что мы узнали?
Коррозия – окисление и разрушение металла под воздействием окружающей среды. Процесс окисления может происходить в присутствии или в отсутствии электролитов. Коррозия, возникающая без воздействия электролитов, называется химической. На поверхности металлов возникают оксиды, гидроксиды, соли. Под действием электролитов возникает электрохимическая коррозия. Окислению подвергается металл, выступающий в роли анода.
Тест по теме
-
Вопрос 1 из 5
Что происходит при коррозии?
- Окисление металла и восстановление корозионной среды
- Восстановление металла и окисление корозионной среды
- Окисление металла и коррозионной среды
- Восстановление металла и коррозионной среды
Начать тест(новая вкладка)
Как проявляется коррозия разных видов
В качестве примера протекания коррозийного процесса можно привести разрушение различных приборов, компонентов автомобилей, а также любых конструкций, произведенных из металла и расположенных:
- в атмосферном воздухе;
- в водах – моря, реки, содержащиеся в почве и под слоями грунта;
- в технических средах и т.д.
В процессе ржавления металл становится многоэлектронным гальваническим элементом. Так, например, если в электролитической среде происходит контакт меди и железа, медь является катодом, а железо – анодом. Отдавая электроны меди, железо в виде ионов попадает в раствор. Ионы водорода начинают двигаться по направлению к меди и там разряжаются. Становясь все более и более отрицательным, катод вскоре приравнивается к потенциалу анода, в результате чего коррозийный процесс начинает замедляться.
Разные виды коррозии проявляются по-разному. Более интенсивно электрохимическая коррозия проявляется в тех случаях, когда в катоде присутствуют вкрапления металла с меньшей активностью по сравнению с корродирующим – на них ржавчина появляется быстрее и является довольно выразительной.
Протекание атмосферной коррозии происходит в условиях влажного воздуха и обычной температуры. В данном случае на поверхности металла образуется пленочка из влаги с растворенным кислородом. Процесс разрушения металла становится интенсивнее по мере увеличения влажности воздуха и содержания газообразных оксидов углерода и серы при условии наличия:
- трещин;
- шероховатостей;
- других факторов, провоцирующих облегчения процесса конденсации.
Почвенная коррозия в наибольшей степени поражает разнообразные подземные сооружения, газопроводы, кабели и другие конструкции. Разрушение меди и других металлов происходит по причине их тесного соприкосновения с почвенной влагой, в составе которой также присутствует растворенный кислород. Разрушение трубопроводов может произойти уже спустя полгода с момента их строительства в том случае, если для почвы, в которой они установлены, характерна повышенная кислотность.
Под воздействием блуждающих токов, исходящих от посторонних объектов, возникает электрическая коррозия. Ее главными источниками являются электрические железные дороги, линии электропередач, а также специальные установки, функционирующие на постоянном электротоке. В большей степени данный вид коррозии провоцирует разрушение:
- газопроводов;
- всевозможных сооружений (мосты, ангары);
- электрокабелей;
- нефтепроводов.
Действие тока провоцирует возникновение участков входа и выхода электронов – то есть, катодов и анодов. Наиболее интенсивным разрушительный процесс является именно на участках с анодами, поэтому на них ржавчина более заметна.
Коррозия отдельных компонентов газопроводов и водяных трубопроводов может быть вызвана тем, что процесс их инсталляции является смешанным, то есть, происходит с использованием различных материалов. Наиболее частыми примерами является точечная коррозия, возникающая в элементах из меди, а также коррозия биметаллов.
При смешанной установке железных элементов со сплавами меди и цинка, процесс коррозии отличается меньшей степенью критичности, чем при медном литье, то есть со сплавами меди, цинка и олова. Предотвратить коррозию трубопроводов можно, используя специальные методы.
Основные виды коррозии
Коррозионные процессы классифицируют по нескольким параметрам, а конкретные типы коррозии различают по некоторым признакам. Ниже вы узнаете, по каким факторам классифицируют коррозию, и что такое, например, химическая коррозия.
Классификация по механизму протекания процессов
Химическая коррозия – процесс контакта элемента металла со средой, способствующей развитию коррозии, во время которого реакция окисления металлического элемента и восстановления самой окислительной компоненты среды происходит одновременно.
Электрохимическая коррозия – механизм реакционного соприкосновения раствора электролита с металлом, сущность которого, в противовес химическому типу ржавления, заключается в процессе, когда атомы металла ионизируются, окислительная компонента среды восстанавливается не в едином пространственном и временном промежутке: скорость реакций обусловлена электродным потенциалом.
Классификация по виду коррозионной среды и условиям
Газовая коррозия – реакция ржавления металлов в условиях газовой среды с минимально допустимым содержанием воды (коэффициент не выше 0,1%) либо с применением экстремально высоких температур. Газовая коррозия популярна в промышленных сферах: нефтехимической, а также химической отраслях.
Подземная коррозия – ржавление в грунтовой среде.
Атмосферная коррозия — ржавление металлов в воздухе либо влажном газе.
Биокоррозия – реакция с появлением ржи под воздействием микроорганизмов.
Контактная коррозия – при подобной реакции участвует несколько металлов с отличными друг от друга потенциалами по электролиту.
Радиационная коррозия – возникновение ржи под влиянием радиоактивных лучей.
Коррозия током – процесс коррозии происходит в условиях воздействия внешнего либо блуждающего тока.
Коррозия под напряжением – ржавление металла в коррозионной среде под механическим напряжением. Химия подобного вида ржи небезопасна, в главной мере для опорных конструкций с воздействием механических нагрузок на них (турбины, рессоры, ведущие оси строений). Немаловажным нюансом при обозначенном типе ржавления служит потенциальная коррозионная усталость – накопительный эффект возникает при периодичном растягивающем напряжении.
Коррозионная кавитация – разрушительное влияние на металл коррозионной среды и ударной силы.
Фреттинг-коррозия – разрушение металлических поверхностей единовременным воздействием благоприятной для ржи среди и вибрации. По проявлению результатов процесса ликвидировать следствие возможно, для этого потребуется четко подобрать структурный материал, снизить уровень трения, применить покрывающую пленку либо выполнить другие подходящие в таком случае действия.
Межкристаллитная коррозия – проявление ржи по граням вкраплений. Так называемое скрытный разлом, в период активности которого внешних признаков не заметно, однако металл в краткие сроки лишается свойств прочности и эластичности. Наиболее часто от подобного вида внешнего вмешательства страдают сплавы, в состав которых входят никель, алюминий, хром.
Щелевая коррозия – является причиной повреждения металла в резьбовых креплениях, между прокладками и аналогичных участках.
На видео: всё о электрохимической коррозии.
Классификация по типу коррозионной деструкции
Сплошная коррозия – ржавчине подвергается поверхность целиком. Различают несколько подтипов:
- Равномерная (поверхностная коррозия) – ржа проявляется одновременно по захваченной процессом территории. Пример – разрушение железных труб на открытом воздухе.
- Неравномерная – скорость реакций на отдельных участках общей территории варьируется.
Избирательная коррозия — ржавеет один из компонентов сплавов или обособленная структурная секция (например, реакция обесцинкования латуни).
Местная коррозия — разрушению подвергаются сепаратные пятна целостного объекта. Проявление наблюдается в форме отдельных вкраплений поврежденностей, проникнувших на малую глубину слоя металла (ржа по латуни в соленой морской воде); значительных углублений в виде раковин (сталь, закопанная в почву); обособленных точек, именуемых питтингами, входящих в толщу металла на серьезную глубину (хромовоникелевая сталь аустенитного класса).
Что такое коррозия?
Слово «коррозия» происходит от латинского «corrodo – грызу». Встречаются ссылки и на позднелатинское «corrosio – разъедание». Но так или иначе:
Хотя коррозию чаще всего связывают с металлами, ей также подвергаются бетон, камень, керамика, дерево, пластмассы. Применительно к полимерным материалам, правда, чаще используется термин деструкция или старение.
Коррозия и ржавчина — не одно и то же
В определении коррозии абзацем выше не зря выделено слово «процесс». Дело в том, коррозию частенько приравнивают к термину «ржавчина». Однако это не синонимы. Коррозия — это именно процесс, в то время как ржавчина — один из результатов этого процесса.
Также стоит отметить, что ржавчина — продукт коррозии исключительно железа и его сплавов (таких как сталь или чугун). Поэтому, когда говорим «ржавеет сталь», то подразумеваем, что ржавеет железо в ее составе.

Если ржавчина относится только к железу, значит другие металлы не ржавеют? Не ржавеют, но это не значит, что они не корродируют. Просто продукты коррозии у них другие.
Например, медь, корродируя, покрывается красивым по цвету зеленоватым налетом (патиной). Серебро на воздухе тускнеет — это на его поверхности образуется налет сульфида, чья тонкая пленка придает металлу характерную розоватую окраску.
 Патина — продукт коррозии меди и ее сплавов
Патина — продукт коррозии меди и ее сплавов
Механизм протекания коррозионных процессов
Разнообразие условий и сред, в которых протекают коррозионные процессы, очень широко, поэтому сложно дать единую классификацию встречающихся случаев коррозии. Но, несмотря на это, все коррозионные процессы имеют не только общий результат — разрушение металла, но и единую химическую сущность — окисление.
Упрощенно окисление можно назвать процессом обмена веществ электронами. Когда одно вещество окисляется (отдает электроны), другое, наоборот, восстанавливается (получает электроны).
Например, в реакции…
… атом цинка теряет два электрона (окисляется), а молекула хлора присоединяет их (восстанавливается).
Частицы, которые отдают электроны и окисляются, называются восстановителями, а частицы, которые принимают электроны и восстанавливаются, называются окислителями. Два этих процесса (окисление и восстановление) взаимосвязаны и всегда протекают одновременно.
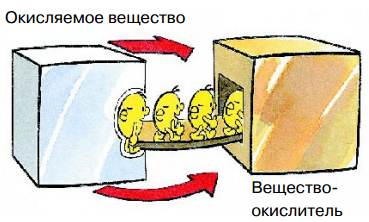
Такие вот реакции, которые в химии называются окислительно-восстановительными, лежат в основе любого коррозионного процесса.
Склонность к окислению у разных металлов неодинакова. Чтобы понять, у каких она больше, а у каких меньше, вспомним школьный курс химии. Было там такое понятие как электрохимический ряд напряжений (активности) металлов, в котором все металлы расположены слева направо в порядке повышения «благородности».
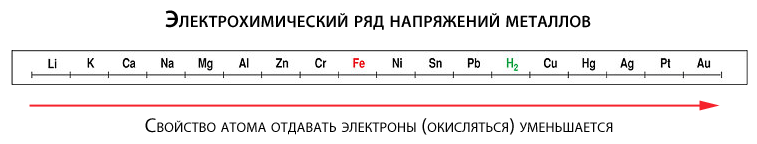
Так вот, металлы, расположенные в ряду левее, более склонны к отдаче электронов (а значит и к окислению), чем металлы, стоящие правее. Например, железо (Fe) больше подвержено окислению, чем более благородная медь (Cu). Отдельные металлы (например, золото), могут отдавать электроны только при определенных экстремальных условиях.
К ряду активности вернемся немного позже, а сейчас поговорим об основных видах коррозии.
МЕТОДЫ ЗАЩИТЫ ОТ КОРРОЗИИ, ИХ ЭФФЕКТИВНОСТЬ
Существуют многочисленные способы защитить металл от разрушений или ржавчины. Выбор того или иного способа определяется конкретными условиями работы и хранения металлических изделий. Наиболее широко применяются: легирование сталей, нанесение металлических покрытий, электрохимическая защита.
Легирование эффективнее всего в условиях воздействия механических напряжений и коррозийной среды. Легирование позволяет предотвратить и коррозийное растрескивание изделий.
Так, например, к группе сталей с особыми химическими свойствами относят коррозионно-стойкие стали. Их получают путем введения в углеродистые и низколегированные стали значительных добавок хрома или хрома и никеля. При содержании хрома 13, 17 и 25% хромистые стали являются не только коррозионно-, но и жаростойкими. Хромоникелевые стали обладают большей коррозионной стойкостью, чем хромистые, и находят широкое применение в химической промышленности.
Металлические покрытия наносят на поверхность изделия тонким слоем металла, обладающего достаточной стойкостью в данной среде. Такое покрытие придает также поверхностным слоям металлоизделий требуемую твердость, износостойкость. Различают два типа покрытий – анодное и катодное. Для железоуглеродистых сплавов таким анодным покрытием может служить покрытие из цинка и кадмия. В воде и во влажном воздухе цинк покрывается слоем основной углекислой соли белого цвета, защищающим его от дальнейшего разрушения. Широкое применение получили цинковые покрытия для защиты арматуры, труб и резервуаров от действия воды и горячих жидкостей.
Металлические покрытия наносят различными способами. Наиболее часто применяется горячий метод, гальванизация и металлизация.
При горячем методе изделие погружают в расплавленный металл, который смачивает его поверхность и покрывает тонким слоем. Затем изделие вынимают из ванны и охлаждают. Таким методом изделие покрывают слоем олова или цинка. Лужение применяют при изготовлении белой жести, при устройстве покрытий на внутренних поверхностях пищевых котлов и других изделий. Цинкованием предохраняют от коррозии, например, кровельное железо, водопроводные трубы.
При гальваническом способе металлические изделия помещают в гальваническую ванну. Под действием электрического тока на поверхности изделия происходит катодное осаждение пленки защитного металла. Толщину покрытия можно регулировать в широких пределах. Покрытия получают также распылением расплавленного металла с помощью специальных металлизационных пистолетов и напылением на его поверхность защищаемого металла. Этот вид защиты используют для крупногабаритных конструкций: ж/д мостов и т. д. В качестве защитного металла используют алюминий, цинк, хром, коррозионно-стойкие стали.
Неметаллические покрытия выполняются из лаков, красок, эмалей и др. веществ и изолируют изделие от воздействия внешней среды. Они легко наносятся на изделие, хорошо закрывают поры, не изменяют свойств металла и являются относительно дешевыми. При хранении и перевозке металлические изделия покрывают специальными смазочными материалами, минеральными маслами и жирами. Для защиты изделий, работающих в высокоагрессивных средах, применяют пластмассовые покрытия из винипласта, поливинилхлорида.
Химические покрытия – защитные оксидные и иные пленки – создаются при воздействии на металл сильных химических реагентов. Широко применяются также оксидирование и фосфатирование металлоизделий.
Оксидирование – создание на поверхности изделия оксидной пленки, обладающей большой коррозийной стойкостью. Наиболее широко применяется для защиты от коррозии изделий из алюминия и его сплавов.
Фосфатирование стальных изделий заключается в создании поверхностного слоя из фосфатов марганца и железа. Фосфатные покрытия используются в дальнейшем в качестве подслоя, часто в сочетании со смазочными материалами, для уменьшения трения при обработке металлов давлением, волочением, для хорошей приработки трущихся деталей машин.
В отдельных случаях прибегают к защите металлов от коррозии при помощи протекторов. Сущность протекторной защиты заключается в том, что к поверхности защищаемого изделия прикрепляют протекторы – куски металла. Образуется гальваническая пара, в которой анод – протектор, катод – изделие. В результате протектор разрушается, защищая изделие. Таким образом защищают, например, подводные металлические части кораблей, прикрепляя к ним пластины цинка.
Виды коррозии
Как уже говорилось, критериев классификация коррозионных процессов существует множество. Так, различают коррозию по виду распространения (сплошная, местная), по типу коррозионной среды (газовая, атмосферная, жидкостная, почвенная), по характеру механических воздействий (коррозионное растрескивание, явление Фреттинга, кавитационная коррозия) и так далее.
Но основным способом классификации коррозии, позволяющим наиболее полно объяснить все тонкости этого процесса, является классификация по механизму протекания.
По этому критерию различают два вида коррозии:
- химическую
- электрохимическую
Химическая коррозия
Химическая коррозия отличается от электрохимической тем, что протекает в средах, не проводящих электрический ток. Поэтому при такой коррозии разрушение металла не сопровождается возникновением электрического тока в системе. Это обычное окислительно-восстановительное взаимодействие металла с окружающей средой.
Наиболее типичным примером химической коррозии является газовая коррозия. Газовую коррозию еще называют высокотемпературной, поскольку обычно она протекает при повышенных температурах, когда возможность конденсации влаги на поверхности металла полностью исключена. К такому виду коррозии можно отнести, например, коррозию элементов электронагревателей или сопел ракетных двигателей.
Скорость химической коррозии зависит от температуры — при ее повышении коррозия ускоряется. Из-за этого, например, в процессе производства металлического проката, во все стороны от раскаленной массы разлетаются огненные брызги. Это с поверхности металла скалываются частички окалины.
Окалина — типичный продукт химической коррозии, — оксид, возникающий в результате взаимодействия раскаленного металла с кислородом воздуха.
Помимо кислорода и другие газы могут обладать сильными агрессивными свойствами по отношению к металлам. К таким газам относятся диоксид серы, фтор, хлор, сероводород. Так, например, алюминий и его сплавы, а также стали с высоким содержанием хрома (нержавеющие стали) устойчивы в атмосфере, которая содержит в качестве основного агрессивного агента кислород. Но картина кардинально меняется, если в атмосфере присутствует хлор.
В документации к некоторым антикоррозионным препаратам химическую коррозию иногда называют «сухой», а электрохимическую — «мокрой». Однако химическая коррозия может протекать и в жидкостях. Только в отличие от электрохимической коррозии эти жидкости — неэлектролиты (т.е. не проводящие электрический ток, например спирт, бензол, бензин, керосин).
Примером такой коррозии является коррозия железных деталей двигателя автомобиля. Присутствующая в бензине в качестве примесей сера взаимодействует с поверхностью детали, образуя сульфид железа. Сульфид железа очень хрупок и легко отслаивается, освобождая свежую поверхность для дальнейшего взаимодействия с серой. И так, слой за слоем, деталь постепенно разрушается.
Электрохимическая коррозия
Если химическая коррозия представляет собой не что иное, как простое окисление металла, то электрохимическая — это разрушение за счет гальванических процессов.
В отличие от химической, электрохимическая коррозия протекает в средах с хорошей электропроводностью и сопровождается возникновением тока. Для «запуска» электрохимической коррозии необходимы два условия: гальваническая пара и электролит.
В роли электролита выступает влага на поверхности металла (конденсат, дождевая вода и т.д.). Что такое гальваническая пара? Чтобы понять это, вернемся к ряду активности металлов.
Смотрим. Cлева расположены более активные металлы, справа — менее активные.
Если в контакт вступают два металла с различной активностью, они образуют гальваническую пару, и в присутствии электролита между ними возникает поток электронов, перетекающих от анодных участков к катодным. При этом более активный металл, являющийся анодом гальванопары, начинает корродировать, в то время как менее активный коррозии не подвергается.
Схема гальванического элемента
Для наглядности рассмотрим несколько простых примеров.
Допустим, стальной болт закреплен медной гайкой. Что будет корродировать, железо или медь? Смотрим в ряд активности. Железо более активно (стоит левее), а значит именно оно будет разрушаться в месте соединения.
Стальной болт — медная гайка (корродирует сталь)
А если гайка алюминиевая? Снова смотрим в ряд активности. Здесь картина меняется: уже алюминий (Al), как более активный металл, будет терять электроны и разрушаться.
Таким образом, контакт более активного «левого» металла с менее активным «правым» усиливает коррозию первого.






